Ilmu Alamiah Dasar
Fisika dan Kimia


a. Fisika




- PENGERTIAN FISIKA DAN KIMIA


Pengertian
Fisika Secara Umum
Fisika
berasal dari kata bahasa Yunani yang berarti “alam”. Fisika ialah salah satu
ilmu pengetahuan alam dasar yang banyak digunakan sebagai dasar bagi ilmu-ilmu
yang lain. Fisika Merupakan ilmu yang mempelajari gejala alam secara
keseluruhan. Fisika mempelajari materi, energi, dan fenomena atau kejadian
alam, baik yang bersifat makroskopis (berukuran besar, seperti gerak Bumi
mengelilingi Matahari) maupun yang bersifat mikroskopis (berukuran kecil,
seperti gerak elektron mengelilingi inti) yang berkaitan dengan perubahan zat
atau energi.
Bidang
fisika secara umum terbagi atas 2 kelompok, yaitu 1. fisika klasik dan 2.
fisika modern. Fisika klasik bersumber pada gejala-gejala yang ditangkap oleh
indra. Fisika klasik meliputi mekanika, listrik magnet, panas, bunyi, optika,
dan gelombang yang menjadi perbatasan antara fisika klasik dan fisika modern.
Fisika modern berkembang mulai abad ke-20, sejak penemuan teori relativitas
Einstein dan radioaktivitas oleh keluarga Curie.
Pengertian
Fisika Menurut Para Ahli
1.
Bambang Ruwanto
Menurut
Bambang Ruwanto Fisika adalah bagian dari ilmu dasar atau sains dan ialah salah
satu ilmu yang fundamental.
2.
Gerthsen (1958)
Menurut
Gerthsen fisika merupakan sebagai suatu teori yang menerangkan gejala-gejala
alam sesederhana mungkin dan berusaha menemukan hubungan antara
kenyataan-kenyataannya. Permasalahan dasar untuk memecahkan persoalannya ialah
mengamati gejala-gejala tersebut.
3.
Young, Hough D
Menurut
Young, Hough D fisika merupakan salah satu ilmu yang sangat dasar dari berbagai
ilmu pengetahuan.
b. Kimia
Pengertian
Kimia Secara Umum
Kimia
menurut asal katanya sebenarnya berasal dari istilah bahasa arab kimiya yang
berarti perubahan materi atau benda. Kimia juga berasal dari bahasa yunani
“khemia” Kimia adalah ilmu yang mempelajari zat/materi, perubahan zat (reaksi),
beserta energi yang menyertainya, dan juga zat baru yang muncul. Perubahan zat
di sini hanyalah perubahan zat secara kimia. Ditandai dengan munculnya zat
baru. Untuk perubahan fisik (mencair, membeku, menguap, dll) tidak dipelajari
dalam kimia.
Kimia secara teori ilmu, kimia adalah ilmu yang mempelajari mengenai komposisi
dan sifat zat atau materi dari skala atom hingga molekul serta perubahan serta
interaksi (reaksi) mereka untuk membentuk materi baru yang ada di sekitar kita.
- SIFAT FISIKA DAN KIMIA
Sifat
fisika adalah perubahan yang dialami suatu benda tanpa membentuk zat baru.
Sifat
ini dapat diamati tanpa mengubah zat-zat penyusun materi tersebut. Sifat fisika
antara lain wujud zat, warna, bau, titik leleh, titik didih, massa jenis,
kekerasan, kelarutan, kekeruhan, kemagnetan, dan kekentalan. Berikut ini
pembahasan mengenai sifat-sifat fisika tersebut :
Wujud
zat
Wujud
zat dibedakan atas zat padat, cair, dan gas. Zat tersebut dapat berubah dari
satu wujud ke wujud lain. Beberapa peristiwa perubahan yang kita kenal, yaitu :
menguap, mengembun, mencair, membeku, meyublim, dan mengkristal.
Warna
Setiap
benda memiliki warna yang berbeda-beda. Warna merupakan sifat fisika yang dapat
diamati secara langsung. Warna yang dimiliki suatu benda merupakan ciri
tersendiri yang membedakan
antara zat satu dengan zat lain. Misal, susu berwarna putih, karbon berwarna
hitam, paku berwarna kelabu pudar dan lain–lain.
Kelarutan
Kelarutan
suatu zat dalam pelarut tertentu merupakan sifat fisika. Air merupakan zat
pelarut untuk zat-zat terlarut. Tidak semua zat dapat larut dalam zat pelarut.
Misal, garam dapat larut dalam air, tetapi kopi tidak dapat larut dalam air.
Daya
hantar listrik
Daya
hantar listrik merupakan sifat fisika. Benda yang dapat menghantarkan listrik
dengan baik disebut konduktor, sedangkan benda yang tidak dapat menghantarkan
listrik disebut isolator. Benda logam pada umumnya dapat menghantarkan listrik.
Daya hantar listrik pada suatu zat dapat diamati dari gejala yang
ditimbulkannya. Misal, tembaga dihubungkan dengan sumber tegangan dan sebuah
lampu. Akibat yang dapat diamati adalah lampu dapat menyala.
Kemagnetan
Berdasarkan
sifat kemagnetan, benda digolongkan menjadi dua yaitu benda magnetik dan benda
non magnetik. Benda magnetik adalah benda yang dapat ditarik kuat oleh magnet,
sedangkan benda non magnetik adalah benda yang tidak dapat ditarik oleh magnet.
Titik
Didih
Titik
didih merupakan suhu ketika suatu zat mendidih.
Titik
Leleh
Titik
leleh merupakan suhu ketika zat padat berubah menjadi zat cair.
b. Kimia
Sifat
kimia adalah perubahan yang dialami suatu benda yang membentuk zat baru.
Ciri-ciri suatu zat yang berhubungan dengan
terbentuknya zat jenis baru. Contoh sifat kimia antara lain mudah terbakar,
mudah busuk, mudah meledak , beracun, dan berkarat (korosif). Berikut
ini pembahasan mengenai sifat-sifat kimia :
Mudah
terbakar
Bensin
termasuk zat yang mudah terbakar. Sehingga, di stasiun pengisian bahan bakar
terdapat larangan “DILARANG MEROKOK“. Dengan mengetahui sifat dari bahan-bahan
yang mudah terbakar, kita akan dapat menggunakannya secara aman.
Mudah
busuk
Akibat
terjadi reaksi kimia dalam suatu makanan atau minuman, dapat mengakibatkan
makanan dan minuman tersebut membusuk dan berubah rasa menjadi asam. Misal,
nasi yang dibiarkan berhari–hari bereaksi dengan udara menjadi basi, susu yang
berubah rasa menjadi asam.
Berkarat
Reaksi
antara logam dan oksigen dapat mengakibatkan benda tersebut berkarat. Logam,
seperti : besi dan seng memiliki sifat mudah berkarat.
Mudah
meledak
Interaksi
zat dengan oksigen di alam ada yang mempunyai sifat mudah meledak, seperti :
magnesium, uranium dan natrium.
Racun
Terdapat
beberapa zat yang memiliki sifat kimia beracun, antara lain: insektisida,
pestisida, fungisida, herbisida dan rodentisida. Zat beracun tersebut digunakan
manusia untuk membasmi hama, baik serangga maupun tikus.
- PERUBAHAN FISIKA DAN KIMIA
Perubahan
Fisika adalah perubahan zat yang tidak menghasilkan zat baru dan bersifat
sementara. Contoh: es mencair, lilin meleleh, pelarutan gula dalam air, dan
lain-lain.
Ciri-Ciri
Perubahan Fisika:
-
Perubahan zat hanya terjadi pada wujudnya, tetapi tidak pada sifatnya
-
Zat hasil perubahan fisika dapat dikembalikan ke bentuk semula
-
Sifat zat yang dimiliki sebelum dan sesudah perubahan sama.
Macam-Macam
Perubahan Fisika
1.
Perubahan Fisika yang berupa perubahan wujud zat.
Perubahan
wujud zat karena pengaruh perubahan suhu/temperatur lingkungan. Lebih jelasnya
dapat dilihat pada gambar dibawah ini:

Keterangan:
-
Mencair, contoh: es mencair dan lilin meleleh
-
Membeku, contoh: air menjadi es dan cairan logam yang membeku
-
Mengembun, contoh: uap menjadi air, terjadinya embun pada pagi hari
-
Menguap, contoh: air yang dipanaskan diatas kompor lambat laun akan menguap
-
Menyublim, contoh: kapur barus padat berubah menjadi gas
-
Menyublim/deposisi, contoh: gas dari kapur barus dapat dipadatkan lagi dengan
metode kristalisasi
2.
Perubahan Fisika yang berupa perubahan ukuran suatu zat.
Materi
yang berukuran besar dapat diperkecil dengan cara mekanik, seperti dipecah,
dipotong, digiling, dll. Contoh: biji kopi ditumbuk menjadi serbuk kopi dan
beras ditumbuk menjadi tepung beras.
3.
Perubahan Fisika yang berupa perubahan volume
Perubahan
volume yang disebabkan oleh penyusutan materi karena didinginkan atau pemuaian
materi karena dipanaskan. Contoh: proses pemuaian rel kereta api di siang hari
karena panas dan penyusutan karena dingin.
4.
Perubahan Fisika yang berupa perubahan bentuk zat.
Perubahan
bentuk materi dapat terjadi jika dipukul, diremas, atau menggunakan alat bantu
seperti mesin. Contoh: kayu yang berasal dari pohon dapat diubah bentuknya
menjadi meja, kursi dan lemari dengan menggunakan alat seperti pahat, gergaji
atau palu, Tanah liat dapat diubah menjadi hiasan didalam rumah, seperti guci,
vas bunga, dll.
b. Kimia
Perubahan
Kimia adalah perubahan suatu zat yang terjadi karena reaksi kimia sehingga
menghasilkan suatu zat baru. Contoh: kertas dibakar menjadi abu, peristiwa
perkaratan besi, dll.
Ciri-Ciri
Perubahan Kimia
-
Terjadi perubahan susunan molekul
-
Terbentuk zat baru dengan sifat zat yang berbeda dengan sifat penyusunnya
-
Perubahan zat bersifat irreversibel (tidak dapat kembali ke bentuk semula).
Macam-Macam
Perubahan Kimia
1.
Perubahan kimia yang menghasilkan perubahan suhu
Proses
Perubahan suhu dibagi menjadi dua, yaitu:
-
Reaksi Eksoterm, yaitu reaksi kimia yang menghasilkan energi panas (kalor)
sehingga meningkatkan suhu lingkungan. Contoh: proses pembakaran petasan,
pembuatan api unggun
-
Reaksi endoterm, yaitu reaksi kimia yang memerlukan (menyerap) energi panas
sehingga menimbulkan efek dingin pada lingkungan. Contoh: garam dapur (NaCl)
yang dilarutkan dalam air.
2.
Perubahan Kimia yang menghasilkan perubahan warna
Terjadinya
perbedaan warna antara sebelum dan sesudah reaksi pada zat-zat yang bereaksi
juga menunjukan adanya perubahan kimia. Contoh: perubahan warna pada kertas
lakmus, kertas lakmus biru saat dicelupkan ke larutan asam akan berubah menjadi
merah, sedangkan kertas lakmus merah saat dicelupkan ke dalam larutan basa akan
berubah menjadi biru.
3.
Perubahan kimia yang dapat menghasilkan gas
Terbentuknya
gas pada proses reaksi adalah salah satu indikator perubahan kimia. Contoh:
logam seng (Zn) yang direaksikan dengan larutan asam sulfat (H2SO4) akan
terbentuk seng sulfat (ZnSO4) dan sejumlah gelembung-gelembung gas hidrogen.
4.
Perubahan kimia yang dapat menghasilkan endapan
produk
dari zat-zat yang bereaksi jik terbentuk endapan maka termasuk perubahan kimia.
Contoh: perak nitrat (AgNO3) dicampur dengan natrium klorida (NaCl)
menghasilkan natrium nitrat (NaNO3) dan endapan berwarna putih perak klorida
(AgCl).
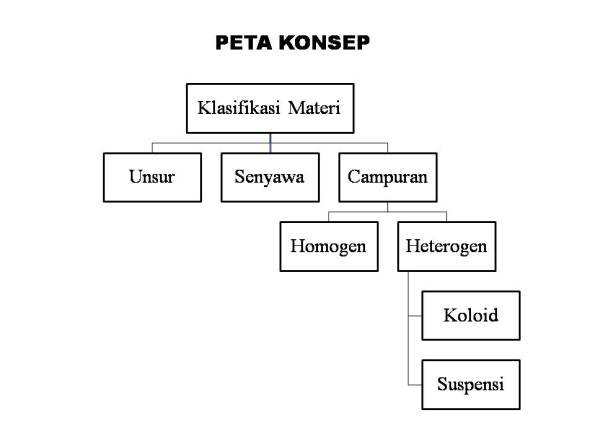
- KLASIFIKASI FISIKA DAN KIMIA

A.
UNSUR
Konsep:
Unsur adalah zat tunggal yang tidak dapat diuraikan lagi menjadi zat lain
dengan reaksi kimia biasa.
Materi
tersusun dari beberapa partikel penyusun. Para ilmuwan mengklasifikasikan zat
atau materi menjadi dua kelompok, yaitu: zat tunggal dan campuran. Unsur dan
senyawa termasuk dalam golongan zat tunggal. Nah, apa yang dimaksud dengan
unsur? Unsur terdiri dari logam dan non logam.
Zat
murni memiliki sifat yang membedakan dengan zat lainnya. Misal, unsur hidrogen
hanya tersusun dari atom-atom hidrogen saja. Unsur oksigen hanya tersusun dari
atom-atom oksigen saja. Sifat oksigen dan hidrogen tidak tampak pada zat yang
dibentuk dari keduanya, misal air (H2O). Di alam terdapat 92 jenis unsur alami,
sedangkan selebihnya adalah unsur buatan. Jumlah keseluruhan unsur di alam
kira-kira 106 jenis unsur. Unsur dikelompokkan menjadi tiga (3) bagian, yaitu :
1.
Unsur logam
Secara
umum unsur logam memiliki sifat berwarna putih mengkilap, mempunyai titik lebur
rendah, dapat menghantarkan arus listrik, dapat ditempa dan dapat menghantarkan
kalor atau panas. Pada umumnya logam merupakan zat padat, namun terdapat satu
unsur logam yang berwujud cair yaitu air raksa. Beberapa unsur logam yang
bermanfaat dalam kehidupan sehari–hari, antara lain:
a.
Khrom (Cr) Digunakan untuk bumper mobil, dan campuran dengan baja menjadi
stainless steel.
b.
Besi (Fe) Merupakan logam yang paling murah, sebagai campuran dengan karbon
menghasilkan baja untuk konstruksi bangunan, mobil dan rel kereta api.
c.
Nikel ( Ni ) Nikel padat sangat tahan terhadap udara dan air pada suhu biasa,
oleh karena itu nikel digunakan sebagai lapisan pelindung dengan cara disepuh.
d.
Tembaga (Cu) Tembaga banyak digunakan pada kabel listrik, perhiasan, dan uang
logam. Campuran tembaga dengan timah menghasilkan perunggu sedangkan campuran
tembaga dengan seng menghasilkan kuningan.
e.
Seng (Zn) Seng dapat digunakan sebagai atap rumah, perkakas rumah tangga, dan
pelapis besi untuk mencegah karat.
f.
Platina (Pt) Platina digunakan pada knalpot mobil, kontak listrik, dan dalam
bidang kedokteran sebagai pengaman tulang yang patah.
g.
Emas (Au) Emas merupakan logam sangat tidak reaktif, dan ditemukan dalam bentuk
murni. Emas digunakan sebagai perhiasan dan komponen listrik berkualitas
tinggi. Campuran emas dengan perak banyak digunakan sebagai bahan koin.
2.
Unsur non logam
Pada
umumnya unsur non logam memiliki sifat tidak mengkilap, penghantar arus listrik
yang buruk, dan tidak dapat ditempa. Secara umum non logam merupakan penghantar
panas yang buruk, namun terdapat satu unsur non logam yang dapat menghantarkan
panas dengan baik yaitu grafit. Beberapa unsur non logam yang bermanfaat dalam
kehidupan sehari–hari, antara lain:
a.
Fluor (F) Senyawa fluorid yang dicampur dengan pasta gigi berfungsi menguatkan
gigi, freon – 12 sebagai pendingin kulkas dan AC.
b.
Brom (Br) Senyawa brom digunakan sebagai obat penenang saraf, film fotografi,
dan bahan campuran zat pemadam kebakaran
c.
Yodium (I) Senyawa yodium digunakan sebagai antiseptik luka, tambahan yodium
dalam garam dapur, dan sebagai bahan tes amilum (karbohidrat) dalam industri
tepung
3.
Unsur semi logam (Metaloid)
Unsur
semi logam memiliki sifat antara logam dan non logam. Beberapa unsur semi logam
yang bermanfaat dalam kehidupan sehari–hari, antara lain :
a.
Silikon (Si) Terdapat di alam terbanyak kedua setelah oksigen, yakni 28 %dari
kerak bumi. Senyawa silikon banyak digunakan dalam peralatan pemotong dan
pengampelasan, untuk semi konduktor, serta bahan untuk membuat gelas dan
keramik.
b.
Germanium ( Ge ) Keberadaan germanium di alam sangat sedikit, diperoleh dari
batu bara dan batuan seng pekat. Germanium merupakan bahan semikonduktor, yaitu
pada suhu rendah berfungsi sebagai isolator sedangkan pada suhu tinggi sebagai
konduktor.
Seorang
ahli kimia yang bernama Demitri Mendleev (1834 ~ 1907) mengajukan susunan tabel
sistem periodik unsur-unsur. Bagaimanakah nama dan lambang unsur dituliskan?
Banyaknya unsur yang terdapat di alam cukup menyulitkan kita untuk
mengingat-ingat nama unsur. Oleh karena itu, diperlukan suatu tata cara untuk
memudahkan kita mengingat nama unsur tersebut.
Jons
Jacob Berzelius (1779 ~ 1848), memperkenalkan tata cara penulisan nama dan
lambang unsur, yaitu :
1.
Setiap unsur dilambangkan dengan satu huruf yang diambil dari huruf awal nama
unsur tersebut.
2.
Lambang unsur ditulis dengan huruf kapital.
3.
Untuk unsur yang memiliki huruf awal sama, maka penulisan nama dibedakan dengan
cara menambah satu huruf di belakangnya dan ditulis dengan huruf kecil.
Contoh:
Unsur Karbon ditulis C, oksigen ditulis O, Aluminium ditulis Al, Kalsium
ditulis Ca.

B.
SENYAWA
Konsep:
Senyawa adalah gabungan dari beberapa unsur yang terbentuk melalui reaksi
kimia.
Senyawa
memiliki sifat yang berbeda dengan unsur-unsur penyusunnya. Misal, dua atom
hidrogen dengan satu atom oksigen dapat bergabung membentuk molekul air (H2O).
Hidrogen adalah gas yang sangat ringan dan mudah terbakar, sedangkan oksigen
adalah gas yang terdapat di udara yang sangat diperlukan tubuh kita untuk
pembakaran.
Tampak
jelas bahwa sifat air berbeda dengan sifat hidrogen dan oksigen. Contoh lain
senyawa adalah garam dapur (NaCl). Garam dapur disusun oleh unsur natrium dan
unsur klor. Natrium memiliki sifat logam yang ringan, sedangkan klor adalah
suatu gas beracun. Dua unsur tersebut digabung membentuk garam dapur berupa
mineral yang sangat dibutuhkan oleh tubuh kita.
Senyawa
termasuk zat tunggal yang tersusun dari beberapa unsur dengan perbandingan
massa tetap. Di alam ini terdapat kurang lebih 10 juta senyawa. Air (H2O)
merupakan senyawa paling banyak terdapat di alam.
Angka
indeks Na = 1, angka indeks Cl = 1, Jadi rumus kimia senyawa tersebut adalah
NaCl ( Natrium klorida ).
Rumus
kimia dapat berupa rumus molekul dan rumus empiris. Rumus molekul adalah rumus
kimia yang menyatakan jenis dan jumlah atom yang menyusun zat. Misal, C2H4
(Etena), H2O (air). Rumus empiris adalah rumus kimia yang menyatakan
perbandingan terkecil jumlah atom–atom pembentuk senyawa. Misal, rumus kimia C2H4,
maka rumus empiris senyawa tersebut adalah CH2.
Joseph
Lonis Proust (1754~1826) seorang ilmuwan dari Perancis mengemukakan hukum
perbandingan tetap atau sering dikenal dengan hukum Proust, yaitu :
perbandingan berat unsur-unsur penyusun senyawa adalah tetap. Eksperimen yang
dilakukan Proust adalah reaksi antara unsur hidrogen dan oksigen sehingga
terbentuk air (H2O). Dari percobaan yang dilakukan oleh Proust ditarik
kesimpulan bahwa:
1.
Air tersusun dari oksigen dan hidrogen dengan perbandingan massa unsur oksigen
banding hidrogen adalah 8 : 1
2.
Jumlah zat sebelum dan sesudah reaksi adalah tetap.
Senyawa-senyawa
baru ditemukan dan dipisahkan dari tumbuh– tumbuhan. Misal, jeruk diketahui
mengandung vitamin C, setelah dilakukan pemisahan ternyata jeruk mengandung
asam askorbat. Struktur vitamin C ditemukan, maka dilakukan sintesis untuk
membuat vitamin C di laboratorium. Rumus senyawa merupakan gabungan lambang
unsur yang menunjukkan jenis unsur pembentuk senyawa dan jumlah atom
masing-masing unsur. Misal, sukrosa memiliki rumus senyawa C12H22O11. Sukrosa
tersusun dari 12 atom karbon, 22 atom hidrogen, dan 11 atom oksigen.

C.
CAMPURAN
Konsep:
Campuran adalah gabungan beberapa zat dengan perbandingan tidak tetap tanpa
melalui reaksi kimia.
Saat
kamu membuat minuman teh, zat apa sajakah yang dicampur? Saat kamu melarutkan
garam atau gula pasir ke dalam gelas yang berisi air, apa yang dapat kamu
amati? Nah, simak penjelasan berikut! Dalam kehidupan sehari-hari banyak kita
jumpai campuran. Misal, air sungai, tanah, udara, makanan, minuman, larutan
garam, larutan gula, dll. Sifat asli zat pembentuk campuran ada yang masih
dapat dibedakan satu sama lain, ada pula yang tidak dapat dibedakan. Di dalam
udara tercampur beberapa unsur yang berupa gas, antara lain: nitrogen, oksigen,
karbon dioksida dan gas-gas lain. Udara segar yang kita hirup mengandung
oksigen yang lebih banyak daripada udara yang tercemar. Dalam udara juga
tersusun dari beberapa senyawa, antara lain : asap dan debu

Campuran
dikelompokkan menjadi dua bagian, yaitu:
1.
Campuran Homogen
Campuran
antara dua zat atau lebih yang partikel-partikel penyusun tidak dapat dibedakan
lagi disebut campuran homogen. Campuran homogen sering disebut dengan larutan.
Contoh campuran homogen, antara lain: campuran air dengan gula dinamakan
larutan gula, campuran air dengan garam dinamakan larutan garam. Ukuran
partikel dalam larutan memiliki diameter sekitar 0,000000001 m, dan tidak dapat
dilihat dengan mikroskop. Terdapat campuran antara logam dengan logam lain
sehingga terbentuk campuran homogen. Misal, Stainless steel banyak digunakan
untuk keperluan alat-alat kesehatan dan rumah tangga. Stainless steel merupakan
campuran logam besi, krom, dan nikel.
Campuran
logam satu dengan logam lain dinamakan paduan logam. Emas murni merupakan logam
yang lunak, mudah dibengkokkan. Agar emas menjadi keras sehingga sulit untuk
dibengkokkan, maka emas murni tersebut dicampur dengan logam lain yaitu
tembaga. Perhiasan yang dijual memiliki kadar 22 karat, 20 karat atau 18 karat.
Apa arti kalimat tersebut? Emas murni memiliki kadar 24 karat, sedangkan emas
yang sudah dicampur dengan logam tembaga memiliki kadar 22 karat, 20 karat,
atau 18 karat. Semakin sedikit kadar emas yang dimiliki, semakin banyak
kandungan tembaga di dalam emas tersebut. Kadangkala dalam campuran emas dan
tembaga masih dicampur lagi dengan perak. Hal ini dilakukan agar menambah
menarik penampilan emas tersebut. Campuran antara emas, tembaga dan perak
menghasilkan emas berwarna putih yang biasa disebut emas putih.
Jenis
campuran homogen, antara lain: campuran gas dalam gas, campuran gas dalam zat
cair, campuran gas dalam zat padat, campuran zat cair dalam zat cair, dan
campuran zat padat dalam zat cair.
2.
Campuran Heterogen
Campuran
antara dua macam zat atau lebih yang partikel-partikel penyusunnya masih dapat
dibedakan satu sama lainnya disebut campuran heterogen. Contoh campuran
heterogen : tanah, air sungai, makanan, minuman, air laut, adonan kue, adonan
beton cor, dll. Pada campuran heterogen dinding pembatas antar zat masih dapat
dilihat, misal campuran air dengan minyak, campuran besi dan pasir, campuran
serbuk besi dan air, dll. Di dalam campuran heterogen dikelompokkan menjadi dua
bagian, yaitu :
a.
Koloid
Partikel-partikel
pada koloid hanya dapat dilihat dengan mikroskop ultra. Ukuran partikel antara
0,5 m s.d 1 mm. Contoh koloid: susu, asap, kabut, agar-agar.
b.
Suspensi
Partikel-partikel
pada suspensi hanya dapat dilihat dengan mikroskop biasa. Ukuran partikel
antara lebih besar dari 0,3 m. Contoh suspensi: minyak dengan air, air keruh,
dan air kapur.
- CONTOH PENEMUAN UNSUR/SENYAWA DALAM KEHIDUPAN MAKHLUK HIDUP
Nikel
merupakan salah satu jenis unsur kimia yang berbentuk metal dan biasanya
ditambang di daerah – daerah tertentu. nikel sendiri memiliki nomor atom 28
yaang saat ini dalam tabel periodic unsur dilambangkan dengan Ni. Walaupun
merupakan salah satu unsur metal, namun nikel asli yang baru ditambang memiliki
sifat lembek dan dapat dibentuk. Biasanya nikel diolah dengan cara dipadukan
dan dicampurkan dengan logam lain, seperti besi dan krom. Nikel memiliki wana
putih keperakan dan dapat ditempa. Manfaat nikel bagi manusia dalam menunjang
kehidupan sehari harinya sangat banyak.
Nikel
sendiri merupakan salah satu elemen yang membentuk inti bumi. Diketahui
sebanyak 10% inti bumi terbbentuk dari nikel. Karena merupakan salah satu unsur
pembentuk inti bumi, maka nikel cukup sulit ditemui dan ditambang. Biasanya
nikel yang ditambang berasal dari larutan nikel yang berada di laut, dengan
kisaran jumlah sekitar 8 juta ton.
Berikut
ini adalah beberapa fakta umum dari nikel :
Nama
: Nikel / Nickel
Lambang
: Ni
Nomor
atom : 28
Massa
Atom : 58.71 gr/mol
Kepadatan
: 8.9 gr / cm3
Titik
lebur : 1453 C
Titik
Didih : 2913 C
Isotop
: 10
Penemu
: Alex Constedt
Nikel
sendiri di dunia memiliki banyak manfaat dan kegunaan, terutama dalam bidang
industri baja dan kebutuhan hidup sehari – hari.
Apa
saja manfaat dan penggunaan dari nikel?
Manfaat
nikel dalam kehidupan sehari hari cukup banyak bagi manusia, setidaknya ada
berbagai industri yang menggunakan nikel sebagai bahan dasarnya. Berikut ini
adalah beberapa manfaat dan penggunaan dari unsur nikel :
1. Sebagai
bahan campuran dalam pembuatan stainless steel
Besi
biasa atau steel memiliki kecenderungan yang mudah mengalami karat atau stain
ketika mengalami proses osidasi, seperti trkena air ataupun udara. Dengan
menggunakan campura nikel dan juga krom, maka terciptalah jenis besi yang tahan
akan karat, yaitu stainless steel. Stainless steel merupakan jenis besi anti
karat yang sudah sangat populer dan banyak digunakan dalm industry – industry
penyedia barang. Berikut ini beberapa benda dan hasil produksi dari stainless
steel yang akrab dalam kehidupan kita sehari – hari :
-Peralatan
makan, seperti sendok, garpu dan sumpit
-Pembuatan
knalpot motor dan mobil
-Rantai
jam tangan
-Besi
– besi pada konstruksi bangunan
-Peralatan
sanitasi, seperti kran air dan shower.
2. Campuran
pada besi baja
Beberapa
jenis besi baja juga melibatkan nikel dalam pembuatan campurannya. Biasanya
besi baja yang memiliki campuran nikel memiliki kekuatan yang lebih baik
dibandingkan besi baja yang dicampu alumunium. Selain tiu besi baja yang
dicampur nikel juga memiliki ketahan terhadap karat yang lebih baik
dibandingkan besi baja murni, walaupun tidak sebaik stainless steel. Berikut
ini beberapa aplikasi dari besi baja dalam kehidupan sehari – hari
-Sebagai
pembuatan konstruksi jembatan, jalan laying, dan gedung
-Sebagai
rel kereta
3. Pembuatan
koin
Biasanya
mata uang suatu Negara memiliki 2 jenis,yaitu dalam bentuk kertas dan bentuk
koin. Mata uang yang memiliki bentuk koin dibuat dengan menggunakan bahan dasar
yang dicampur dengan unsur nikel. Hal ini dapat membuat uang koin atau yang
biasa dikenal dengan istilah uang logam memiliki daya tahan terhadap karat, dan
juga memiliki tekstur yang mengkilap.
4. Aplikasi
nikel dalam dunia otomotif dan variasi
Apabila
anda seorang pegiat dan orang yang hobi dengan dunia otomotif, pasti sudah
cukup akrab dengan nikel sebagai salah satu pemanis kendaraan. Biasa nikel dan
krom dapat menjadi bahan lapisan tambahan pada part – part otomotif agar
menjadi lebih kinclong dan menarik. Lapisan ini biasanya selain dapat mencegah
munculnya karat, dapat juga menjaga kualitar part agar tidak cepat rusak.
Berikut ini adalah beberapa part otomotif yang sering diaplikasikan campuran
nikel dan krom :
-Velg
-Rangka
-Bumper
-Knalpot
-Bagian
– bagian kecil, seperti pijakan kaki, handle rem dan spion
5. Bahan
baku pembuatan monel
Apa
anda pernah mendengar tentang monel? Monel merupakan salah satu jenis logam
yang merupakan campuran dari nikel dan tembaga. Hal ini dapat menghasilkan
logam yang keras dan kuat, tahan terhadap karat, namun dengan harga yang
relative lebih terjangkau dibandingkan jenis besi yang full stainless.
Biasanya, monel ini dipergunakan sebagai :
-Baling
– baling pada kapal laut
-Sebagai
aksesoris, seperti lionting, rantai kalng, gelang, dan cincin
6. Kawat
Sifat
nikel yang mudah dibentuk membuat unsur ini dapat dibentuk menjadi kawat. Kawat
yang dihasilkan oleh nikel ini memiliki ketahanan yang baik, dan juga memiliki
sifat yang anti karat. Biasanya kawat yang dibuat dari bahan dasar nikel ini
dipergunakan pada turbin mesin jet.
7. Melapisi
senjata
Dengan
sifatnya yang kuat dan anti karat, nikel juga sering dimanfaatkan sebagai
pelapis dari berbagai jennies senjata yang diprodoksi di pabriknya. Dengan
menambahkan lapisan nikel pada senjata, maka kalitas senjata akan bertambah
baik, karena menjadi lebih kuat dan tahan karat serta tidak mudah mengalami
korosi.
8. Menjadi
katalis
Nikel
juga dimanfaatkan sebagai katalis, ang dapat membuat minyak sayur mengalami
hidrogenasi sehingga berubah bentuk menjadi bentuk padat
9. Plating
Beberapa
metode plating atau metoe penyolderan menggunakan bantuan nikel untuk
mlaksanakannya. Nikel memiliki sifat yang mudah melebur, dan dapat melapisi
dengan baik, sehingga beberapa komponen elektronik juga mengandalkan nikel
dalam melakukan plating atau pelapisannya.
10. Baterai
isi ulang
Pemanfaatan
lain dari nikel adalah sebagai bahan dasar dari bateai yang dapat diisi ulang,
alias rechargeable battery. Biasanya baterai yang memilikki bahan dasar nikel
ini adalah baterai aki ataupun baterai kecil yang biasa kita gunakan sehari –
hari.
Walaupun
memiliki banyak manfaat, namun demikian terlalu banyak terkontaminasi dengan
unsur nikel dapat menyebabkan gangguan kesehatan, seperti :
-Kemungkinan
mengalami gejala penyakit paru – paru
-Sakit
kepala dan pusing
-Asma
-Gangguan
jantung
Sumber:
Ani
Winarsih, dkk. 2008. IPA Terpadu untuk SMP/ MTS Kelas VII. Jakarta: Pusat
Perbukuan Departemen Pendidikan Nasional


Komentar
Posting Komentar